Deux injections par an, et une promesse : faire reculer le VIH là où l’observance des comprimés quotidiens s’effondre. Pendant que le Kenya annonce son déploiement dès mars 2026 après réception d’un premier lot, la République démocratique du Congo (RDC) n’a toujours pas franchi le cap. Pourquoi ce décalage, alors que l’OMS recommande déjà le produit et que les essais ont frôlé le “zéro infection” ?
Une molécule née dans les laboratoires de Gilead, devenue “capsid inhibitor” vedette
Le lenacapavir (ancien code GS-6207) est développé par Gilead Sciences et appartient à une classe nouvelle : les inhibiteurs de la capside. La capside est la “coque” protéique du VIH, indispensable à plusieurs étapes de l’infection. Les travaux de chimie médicinale et l’historique de développement décrivent un objectif clair : viser une cible virale moins exploitée afin de contourner certaines résistances aux classes classiques.
Comment il fonctionne dans le corps (propriétés pharmacologiques)
Contrairement aux antirétroviraux qui ciblent surtout l’entrée du virus, la transcriptase inverse, l’intégrase ou la protéase, lenacapavir cible la capside et perturbe plusieurs moments du cycle viral :
- Après l’entrée du VIH, il gêne des mécanismes liés au “déshabillage” (uncoating) et au transport du matériel viral.
- À la production de nouveaux virions, il dérègle l’assemblage/maturation, rendant les particules virales moins aptes à infecter.
Ce caractère “multi-étapes” est l’un des arguments qui expliquent l’intérêt scientifique autour du produit et sa place dans les stratégies chez des patients multirésistants (traitement) et, désormais, dans la prévention (PrEP).
Pharmacocinétique : pourquoi “6 mois” est crédible
La “révolution” du lenacapavir tient moins au slogan qu’à sa pharmacocinétique :
- Formulation injectable sous-cutanée (SC) à longue durée d’action.
- Des concentrations actives maintenues suffisamment longtemps pour envisager un schéma semestriel (deux administrations/an).
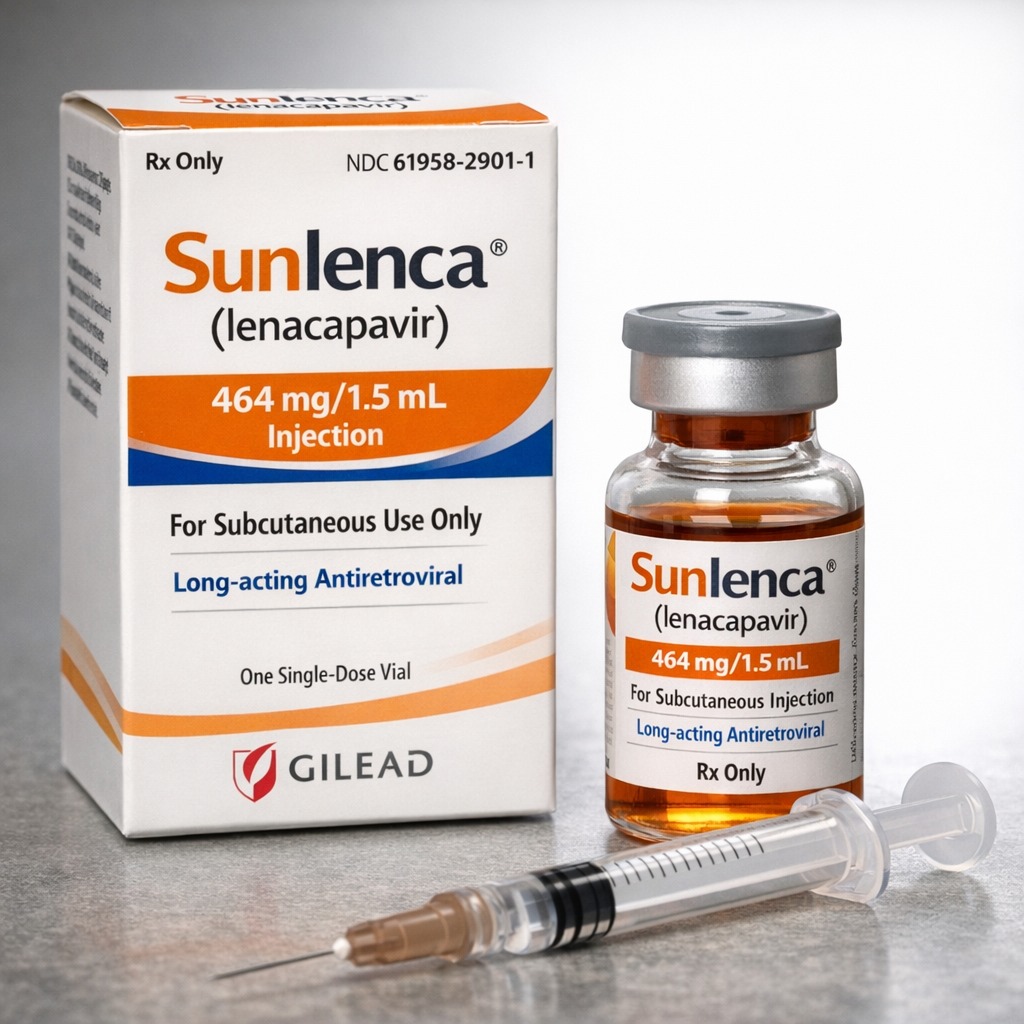
- Dans le cadre du traitement (Sunlenca), la notice FDA décrit des schémas associant une phase orale (lead-in) et une injection SC ensuite, l’objectif étant d’assurer des niveaux thérapeutiques stables chez des patients lourdement pré-traités.
Pour la PrEP, l’idée est la même : tenir la barrière pharmacologique sur la durée, pour que l’efficacité ne dépende pas d’une prise quotidienne (le talon d’Achille de la PrEP orale dans plusieurs populations).
Efficacité clinique : les essais qui ont changé la conversation
PURPOSE 1 : “zéro infection” chez des adolescentes et jeunes femmes
Dans l’essai randomisé de phase 3 PURPOSE 1, mené en Afrique du Sud et en Ouganda, aucune infection VIH n’a été observée dans le bras lenacapavir 2 fois/an au moment de l’analyse principale—un résultat qui a frappé la communauté scientifique.
De la clinique au politique : l’OMS tranche
Le 14 juillet 2025, l’OMS recommande officiellement le lenacapavir injectable comme option additionnelle de prévention dans une approche combinée, en insistant aussi sur l’importance des stratégies de dépistage adaptées aux PrEP injectables.
Sécurité : ce que montrent les données (et ce qu’on surveille)
Les données de sécurité les plus structurées proviennent :
- des essais de traitement chez des patients lourdement pré-traités (CAPELLA) et
- d’essais en populations plus larges (traitement et prévention), avec un suivi continu.
Dans la documentation réglementaire (FDA) du Sunlenca (traitement), les effets indésirables et la tolérance sont décrits sur la base d’essais cliniques (CAPELLA notamment), avec une surveillance standard des événements indésirables et des paramètres biologiques.
En prévention, l’OMS et les synthèses de suivi insistent sur une mise en œuvre avec dépistage et dispositifs de suivi, car toute PrEP injectable à longue durée d’action exige une vigilance : si une infection survient malgré tout, il faut l’identifier tôt pour éviter une exposition “prolongée” à des concentrations décroissantes.
Profil de résistance : l’enjeu silencieux d’un médicament très long-acting
La résistance au lenacapavir est documentée comme liée à des mutations de la capside. Des publications de suivi d’essais rapportent l’apparition de mutations associées à une résistance dans un petit nombre de participants sous certains schémas de traitement (ex. mutations telles que Q67H, K70R rapportées dans des analyses de CALIBRATE).
Point clé (souvent absent des débats publics) : la longue demi-vie est une force, mais aussi un défi programmatique. Plus un médicament “reste longtemps”, plus il faut :
- dépister correctement avant l’initiation,
- organiser un suivi,
- éviter les “retards” dans les ré-injections,
- et disposer d’algorithmes cliniques solides en cas de séroconversion.
Chronologie : de l’invention à l’Afrique, puis jusqu’au Kenya (2026)
- 2022 : FDA approuve Sunlenca (lenacapavir) comme traitement de patients vivant avec un VIH multirésistant et lourdement pré-traités (CAPELLA).
- 2024 : publication majeure dans le New England Journal of Medicine pour la prévention (PURPOSE 1, Afrique du Sud/Ouganda).
- 18 juin 2025 : la FDA approuve lenacapavir pour la prévention (PrEP longue durée) aux États-Unis (dossier appuyé par PURPOSE).
- 14 juillet 2025 : l’OMS recommande lenacapavir injectable comme option de prévention.
- 2024–2025 : Gilead formalise une stratégie d’accès : licences volontaires “royalty-free” avec plusieurs fabricants de génériques pour 120 pays (sous réserve d’autorisations), et accord avec le Fonds mondial pour accélérer l’accès dans des pays soutenus, à prix non lucratif pour Gilead dans ce cadre.
- 17–18 février 2026 : le Kenya annonce avoir reçu un premier lot (21 000 doses) et vise une mise en œuvre dès début mars (15 comtés, puis doses de continuation attendues).
Pourquoi ce n’est pas encore en RDC
À la date d’aujourd’hui (19 février 2026), on ne trouve pas d’annonce publique solide d’enregistrement national ou de déploiement officiel en RDC comparable à ce que le Kenya communique.
Les raisons sont rarement “médicales”. Elles sont presque toujours systémiques :
- Réglementaire : il faut un dossier d’autorisation (ou une voie accélérée) et une décision nationale d’intégration. L’OMS peut recommander, mais un pays doit enregistrer et cadrer l’usage.
- Programmatique : la PrEP injectable exige un dispositif opérationnel :
- calendrier semestriel,
- dépistage compatible PrEP LA,
- chaîne d’approvisionnement,
- formation, pharmacovigilance.
- Financement / achats : même avec les accords (Fonds mondial, licences), il faut que le pays :
- inscrive la ligne budgétaire,
- sécurise l’approvisionnement (branded vs génériques),
- planifie un pilote puis l’extension.
- Priorisation : la RDC a de multiples urgences sanitaires concurrentes ; sans arbitrage national, les innovations restent “hors programme”.
Ce que la RDC doit faire, concrètement (feuille de route)
Si Kinshasa veut éviter d’arriver 2–3 ans après ses voisins, la séquence la plus réaliste ressemble à ceci :
- Décision politique et technique : instruire le PNLS + Autorité de régulation du médicament pour un fast-track fondé sur recommandations OMS + dossiers existants.
- Mise à jour des directives nationales : intégrer lenacapavir comme option de PrEP avec critères d’éligibilité, schémas, protocoles de dépistage et suivi.
- Accord d’accès / achats : négocier via Fonds mondial (RDC est typiquement éligible à ces mécanismes), aligner le quantitatif (doses) et le calendrier.
- Pilote ciblé (6–12 mois) : provinces/axes à incidence élevée + populations clés, avec indicateurs (adhésion, séroconversion, rétention à 6 mois).
- Pharmacovigilance renforcée : circuit de déclaration, gestion des retards de ré-injection, prise en charge si séroconversion (enjeu résistance).
Le vrai test : l’équité d’accès, pas la performance en essai
Le Kenya ne “découvre” pas seulement un médicament ; il teste un modèle : convertir une innovation clinique en politique publique. La RDC, elle, risque un scénario classique : admirer le progrès… et l’importer trop tard, quand l’épidémie a déjà fait son travail.
Africa CDC convoque une réunion régionale d’urgence après l’apparition d’une nouvelle flambée d’Ebola en Ituri
Face au risque de propagation transfrontalière, la RDC, l’Ouganda et le Soudan du Sud mobilisés…
Nord-Kivu : un chercheur congolais développe des lignées de pomme de terre capables de résister à une bactérie qui détruit jusqu’à 100 % des récoltes
À l’Est de la République démocratique du Congo, une maladie silencieuse détruit depuis des années…
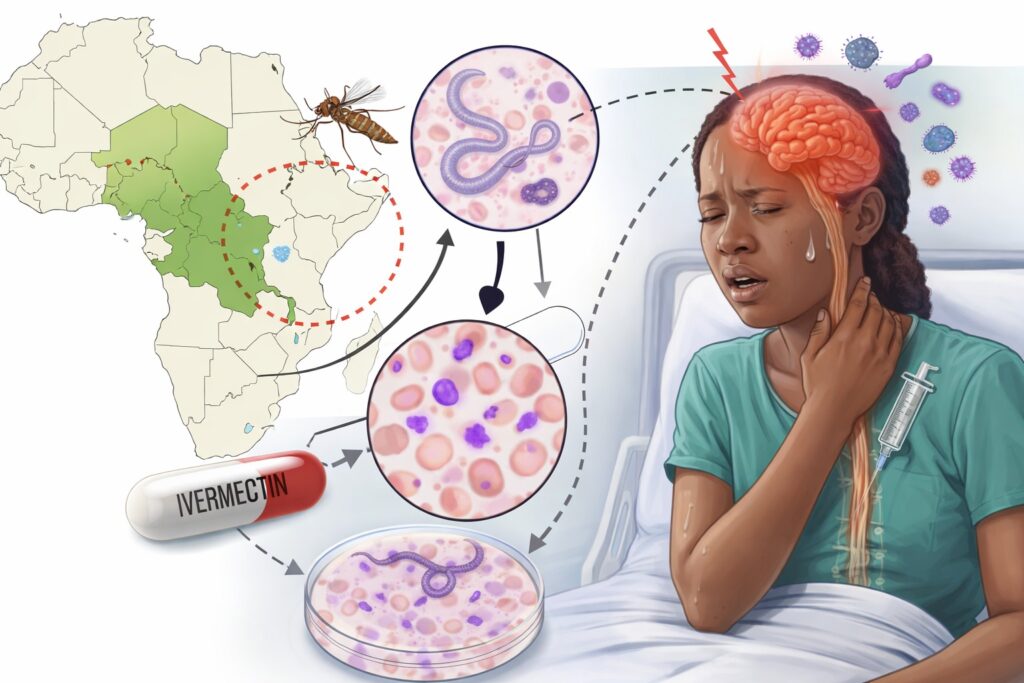
Ivermectine, loase et paludisme : une étude congolaise révèle un risque neurologique critique en Afrique centrale
Dans les zones tropicales d’Afrique centrale, où les maladies parasitaires s’entrecroisent, un traitement peut parfois…
Un chercheur congolais publie dans Science : pourquoi les amphibiens deviennent un enjeu stratégique pour la conservation en Afrique
C’est une avancée scientifique majeure qui mérite d’être soulignée au-delà du cercle académique. Le jeune…
Cancer de la prostate en Afrique centrale et de l’Ouest : une maladie silencieuse, diagnostiquée trop tard
À travers l’Afrique centrale et de l’Ouest, le cancer de la prostate continue de progresser…
À Butembo, le « musoma » s’impose comme une réponse à la crise alimentaire sans compromettre le haricot
À Butembo, le musoma (feuilles de haricot) s’impose comme une alternative alimentaire face à la…